A Agência Nacional de Vigilância Sanitária (Anvisa) divulgou, nesta quarta-feira (22) os pareceres públicos de aprovação da vacina da Pfizer para crianças de 5 a 11 anos de idade. Os documentos são uma resposta ao ministro da Saúde, Marcelo Queiroga, que afirmou que o Governo só iria se manifestar sobre a imunização infantil após análise dos relatórios.
O documento em questão reflete a avaliação de benefício-risco considerada pela Anvisa para aprovar o uso da vacina nessa faixa etária.
A Anvisa aprovou na semana passada uma versão da vacina da Pfizer para crianças de 5 a 11 anos. O governo Bolsonaro, porém, ainda não disse quando os imunizantes vão começar a ser aplicados.
Em nota, a Agência informou que “autorização de vacinas são realizadas por equipes multidisciplinares de especialistas em regulação e vigilância sanitária devidamente capacitados” e que, se tratando especificamente do imunizante infantil, a agência também ouviu entidades médicas a respeito.
“Nessa avaliação, a Agência também contou com a participação das sociedades médicas de notório saber no tema: Sociedade Brasileira de Infectologia (SBI), do Departamento de Infectologia da Sociedade Brasileira de Pediatria (SBP) e do Instituto de Pesquisa do Hospital Albert Einstein, também foi convidada a Sociedade Brasileira de Imunologia (SBI) e da Associação Brasileira de Saúde Coletiva (Abrasco)”, afirmou a Anvisa

Que vacina é essa? Pfizer Biontech
A divulgação dos pareceres público é uma resposta ao ministro da Saúde, Marcelo Queiroga, que afirmou, no dia 20 de dezembro, que “a pressa é inimiga da perfeição” e que ainda esperava documentos da Anvisa para se manifestar.
“Não é um comunicado público que vai fazer o Ministério da Saúde se posicionar de uma maneira ou de outra. Eu preciso de toda a análise. A Análise da qualidade, da evidência científica apresentada, avaliação da amostra de pacientes naquele ensaio clínico. Nós temos que verificar tudo”, declarou Queiroga.
No sábado (18), Queiroga afirmou que o governo só divulgará uma posição oficial sobre a vacinação de crianças entre 5 e 11 anos contra a Covid no próximo dia 5 de janeiro.
De acordo com Queiroga, haverá uma audiência pública, no dia 4 de janeiro no Ministério da Saúde, que servirá de base para a decisão final da pasta.
“Até o dia 5 de janeiro é um tempo absolutamente adequado para que as autoridades possam analisar a decisão da Anvisa em todas as suas nuances, inclusive em relação à aplicação dessas vacinas”, afirmou Queiroga a jornalistas.
Vacina é segura e eficaz, diz Anvisa
Em nota, a Anvisa rebateu novamente o Ministério e afirmou que a vacina da Pfizer é segura e eficaz no combate a Covid-19 em crianças.
“Com base na totalidade das evidências científicas disponíveis, incluindo estudos de fase I, II e III, a Anvisa concluiu que vacina Pfizer-BioNTech Covid-19, quando administrada no esquema de 2 doses em crianças de 5 a 11 anos de idade, é segura e eficaz na prevenção da Covid-19 sintomática, na prevenção das doenças graves, potencialmente fatais ou condições que podem ser causadas pelo SARS-CoV-2″, disse a Anvisa.
Ao contrário do Brasil, diversos países já começaram a vacinar crianças contra a Covid-19. De acordo com um levantamento feito pelo g1, são ao menos 16 nações.
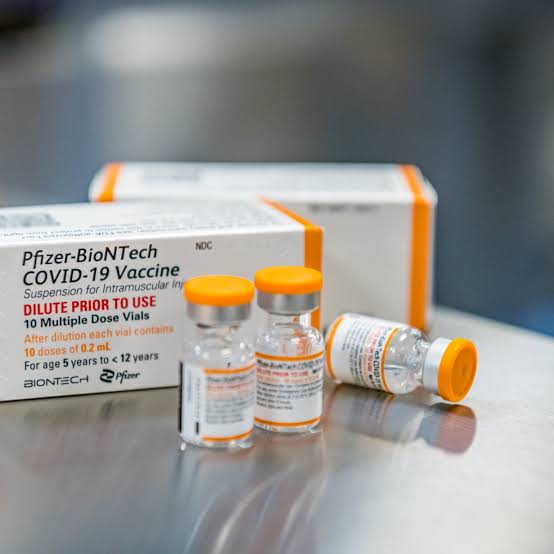
A vacina para este público tem diferenças em relação à que foi aplicada nos adultos. Por isso, o governo federal terá que comprar uma versão específica do produto com dosagens e frascos diferentes (foto acima), apesar de o princípio ativo ser o mesmo.
Em outubro, a Pfizer disse que a vacina é segura e mais de 90,7% eficaz na prevenção de infecções em crianças de 5 a 11 anos. O estudo acompanhou 2.268 crianças de 5 a 11 anos que receberam duas doses da vacina ou placebo, com três semanas de intervalo.
A Anvisa alerta que a autorização é baseada nos dados disponíveis até o momento e os resultados são avaliados a todo momento. Veja as orientações da agência:
- A dose para as crianças entre 5 e 11 anos de idade é 1/3 da formulação já aprovada no Brasil.
- A dosagem é de 10 microgramas.
- A formulação pediátrica é diferente daquela aprovada anteriormente apresentada para o público com mais de 12 anos – portanto, não pode ser utilizada a formulação de adultos diluída.
- A criança que completar 12 anos entre a primeira e a segunda dose deve manter a dose pediátrica.
Não há estudos sobre a coadministração com outras vacinas. Segundo a Anvisa, até que saiam mais estudos, é indicado um intervalo de 15 dias entre a vacina da Covid-19 e outros imunizantes do calendário infantil.
G1