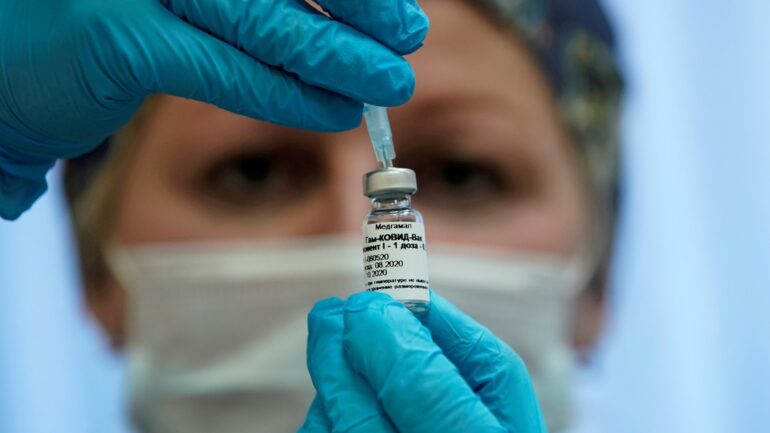
A Rússia concedeu aprovação regulatória a uma segunda vacina contra Covid-19, mostrou o registro de medicamentos autorizados do país nesta quarta-feira (14). O presidente Vladimir Putin deu a notícia em uma reunião de governo.
A vacina foi desenvolvida pelo Instituto Vector, da Sibéria, que concluiu o estágio inicial de testes em humanos em setembro.
“Precisamos aumentar a produção da primeira e da segunda vacina”, disse Putin em comentários transmitidos pela televisão estatal.
A imunização desenvolvida pelo instituto é feita a partir de uma tecnologia criada inicialmente para o Ebola. Ela é composta por fragmentos de proteínas (peptídeos) do vírus que são capazes de estimular o sistema imune a induzir uma resposta protetora.
A Rússia registrou em agosto sua primeira candidata a vacina, desenvolvida pelo Instituto Gamaleya, de Moscou. Os testes em estágio avançado desta candidata com pelo menos 40 mil pessoas estão em andamento.
A vacina, batizada de “Sputnik V” em homenagem ao primeiro satélite do mundo, lançado pela União Soviética, ainda não está em circulação geral.
Etapas para a produção de uma vacina
Para se produzir uma vacina, leva tempo. A mais rápida desenvolvida até o momento foi a vacina contra a caxumba, que precisou de cerca de quatro anos até ser licenciada e distribuída para a população.
Antes de começar os testes em voluntários, a imunização passa por diversas fases de experimentação pré-clinica (em laboratório e com cobaias). Só após ser avaliada sua segurança e eficácia é que começam os testes em humanos, a chamada fase clínica – que são três:
- Fase 1: é uma avaliação preliminar da segurança do imunizante, ela é feita com um número reduzido de voluntários adultos saudáveis que são monitorados de perto. É neste momento que se entende qual é o tipo de resposta que o imunizante produz no corpo. Ela é aplicada em dezenas de participantes do experimento.
- Fase 2: na segunda fase, o estudo clínico é ampliado e conta com centenas de voluntários. A vacina é administrada a pessoas com características (como idade e saúde física) semelhantes àquelas para as quais a nova vacina é destinada. Nessa fase é avaliada a segurança da vacina, imunogenicidade (ou a capacidade da proteção), a dosagem e como deve ser administrada.
- Fase 3: ensaio em larga escala (com milhares de indivíduos) que precisa fornecer uma avaliação definitiva da sua eficácia e segurança em maiores populações. Além disso, feita para prever eventos adversos e garantir a durabilidade da proteção. Apenas depois desta fase é que se pode fazer um registro sanitário.
Segundo a Agência Nacional de Vigilância Sanitária (Anvisa) para se fazer um ensaio clínico no Brasil, é preciso da aprovação do Comissão Nacional de Ética em Pesquisa (Conep), órgão vinculado ao Ministério da Saúde. Os voluntários são recrutados pelos centros de pesquisa.
*Com informações da agência Reuters